Đề cương ôn tập môn Hóa học Lớp 12 - Chuyên đề: Phân biệt một số chất vô cơ
PHẦN II: CÂU HỎI VÀ BÀI TẬP
B1. CẤP ĐỘ BIẾT VÀ HIỂU
Câu 1: Để phân biệt CO2, SO2 người ta dùng
A. dd BaCl2. B. dd Ca(OH)2 dư.
C. Dd nước brom. D. Quì tím.
Câu 2: Cho quì tím vào dung dịch chứa CH3COOH. Quì tím sẽ hóa
A. đỏ B. không đổi màu C. xanh D. trắng
Câu 3: Cho quì tím ẩm lần lượt vào các bình đựng khí NH3, H2S, SO2, CO2. Quì tím sẽ hóa xanh trong bình đựng khí
A. NH3B. H2S C. SO2 D. CO2
Câu 4: Dung dịch chứa Cu2+ thường có màu
A. đỏ. B. vàng. C. xanh. D. trắng.
Câu 5: Để chứng tỏ sự có mặt của ion NO3- trong dd chứa các ion: NH4+, Fe3+, NO3- ta nên dùng thuốc thử là
A. dd AgNO3. B. dd NaOH.
C. dd BaCl2. D. Cu và vài giọt dd H2SO4đặc, đun nóng.
Câu 6:Có 5 lọ đựng riêng biệt các khí sau: N2, NH3, Cl2, CO2, O2. Để xác định lọ đựng khí NH3 chỉ cần dùng thuốc thử duy nhất là
Tóm tắt nội dung tài liệu: Đề cương ôn tập môn Hóa học Lớp 12 - Chuyên đề: Phân biệt một số chất vô cơ
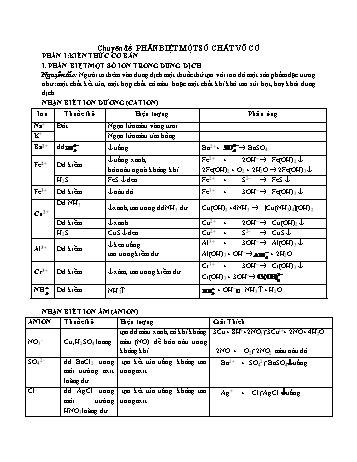
NH Dd kiềm NH3 + OH-NH3 + H2O NHẬN BIẾT ION ÂM (ANION) ANION Thuốc thử Hiện tượng Giải Thích NO3- Cu, H2SO4 loang tạo dd màu xanh, có khí không màu (NO) dễ hóa nâu trong không khí 3Cu + 8H++2NO3-(3Cu2++ 2NO+ 4H2O 2NO + O2( 2NO2 màu nâu đỏ SO42- dd BaCl2 trong môi trường axit loãng dư tạo kết tủa trắng không tan trong axit Ba2+ + SO42-( BaSO4trắng Cl- dd AgCl trong môi trường HNO3 loãng dư tạo kết tủa trắng không tan trong axit Ag+ + Cl-(AgCl trắng CO32- Dung dịch axit và nước vôi trong tạo ra khí làm đục nước vôi trong CO32- + 2H+ ( CO2 + H2O CO2 + Ca(OH)2 (CaCO3trắng + H2O. OH - Quì tím Hóa xanh NHẬN BIẾT MỘT SỐ CHẤT KHÍ Nguyên tắc: Người ta có thể dựa vào tính chất vật lí hoặc tính chất hóa học đặc trưng của nó Khí Thuốc thử Hiện tượng Phản ứng CO2 (không màu, không mùi) dung dịch Ba(OH)2, Ca(OH)2 dư tạo kết tủa trắng CCO2 + Ca(OH)2→ CaCO3 +H2O H2O SO2 (không màu, mùi hắc, độc) dd brom; iot hoặc cánh hoa hồng nhạt màu brom; iot; cánh hoa hồng. SO2 + 2H2O + Br2→ 2HBr + H2SO4 H2S (mùi trứng thối) Giấy lọc tẩm dd muối chì axetat Có màu đen trên giấy lọc H2S + Pb2+→ PbS + 2H+ NH3 (không màu, mùi khai) Giấy quì tím ẩm quì tím chuyển sang màu xanh PHẦN II: CÂU HỎI VÀ BÀI TẬP B1. CẤP ĐỘ BIẾT VÀ HIỂU Câu 1: Để phân biệt CO2, SO2 người ta dùng A. dd BaCl2. B. dd Ca(OH)2 dư. C. Dd nước brom. D. Quì tím. Câu 2: Cho quì tím vào dung dịch chứa CH3COOH. Quì tím sẽ hóa A. đỏ B. không đổi màu C. xanh D. trắng Câu 3: Cho quì tím ẩm lần lượt vào các bình đựng khí NH3, H2S, SO2, CO2. Quì tím sẽ hóa xanh trong bình đựng khí A. NH3B. H2S C. SO2 D. CO2 Câu 4: Dung dịch chứa Cu2+ thường có màu A. đỏ. B. vàng. C. xanh. D. trắng. Câu 5: Để chứng tỏ sự có mặt của ion NO3- trong dd chứa các ion: NH4+, Fe3+, NO3- ta nên dùng thuốc thử là A. dd AgNO3. B. dd NaOH. C. dd BaCl2. D. Cu và vài giọt dd H2SO4đặc, đun nóng. Câu 6:Có 5 lọ đựng riêng biệt các khí sau: N2, N... một dd là A. dd ammoniac. B. không thể thực hiện được. C. dd KOH. D. dd H2SO4 đặc nguội. Câu 13: Chỉ dùng mộtthuốc thử có thể phân biệt được 3 dung dịch: BaCl2,AlCl3, FeCl3 . Thuốc thử đó là: A. Khí CO2 B. dd HCl loãng C. dd BaCl2 D. dd NaOH Câu 14: Để loại bỏ tạp chất Fe, Cu có trong mẫu Ag và không làm thay đổi lượng Ag, người ta ngâm mẫu bạc này vào một lượng dư dd A. AgNO3. B. HCl. C. H2SO4 đặc nguội. D. FeCl3 Câu 15: Có 3 lọ đựng 3 chất bột riêng biệt: Al, Al2O3, Fe. Có thể nhận biết 3 lọ trên bằng 1 thuốc thử duy nhất là: A. dd NaOH. B. H2O. C. dd FeCl2. D. dd HCl. Câu 16: Dùng thuốc thử nào sau đây có thể phân biệt được dung dịch Fe2(SO4)3 và dung dịch Fe2(SO4)3 có lẫn FeSO4 ? A. dung dịch NaOH. B. dung dịch NH3. C. dung dịch KMnO4/H2SO4. D. dung dịch Ba(OH)2. Câu 17: Để thu được Ag tinh khiết từ hỗn hợp bột Ag-Fe, người ta dùng dư hoá chất nào sau đây? A. AgNO3. B. FeCl3. C. CuSO4. D. HNO3 đặc nguội. Câu 18:Có các dung dịch : AlCl3, ZnSO4, FeSO4. Chỉ cần dùng thuốc thử nào sau đây có thể phân biệt được các dung dịch trên? A. Quỳ tím B. Dung dịch NH3 C. Dung dịch NaOH D. Dung dịch BaCl2 B3. CẤP ĐỘ VẬN DỤNG Câu 19: Có 4 dung dịch không màu chứa trong 4 lọ mất nhãn: NaCl, Mg(NO3)2,Al(NO3)3, Fe(NO3)2. Chọn một kim loại nào dưới đây để phân biệt 4 lọ trên? A. Na B. Al C. Fe D. Ag Câu 20: Để phân biệt các dung dịch riêng biệt: NaCl, MgCl2, AlCl3, FeCl3, có thể dùng dung dịch A. HCl. B. Na2SO4. C. NaOH. D. HNO3 Câu 21: Có 4 chất rắn trong 4 lọ riêng biệt gồm NaOH, Al, Mg và Al2O3. Nếu chỉ dùng thêm một thuốc thử để phân biệt 4 chất trên, thuốc thử được chọn là: A. dd HCl. B. dd HNO3 đặc, nguội. C. H2O D. dd KOH Câu 22: Một học sinh đề nghị các cách để nhận ra lọ chứa khí NH3 lẫn trong các lọ riêng biệt chứa các khí N2, O2, Cl2, CO2 là:... dùng thêm quỳ tím thì số lượng dung dịch có thể phân biệt được là A. 6. B. 4. C. 2. D. 3. Câu 27: Có 5 dung dịch chứa từng chất riêng rẽ sau: BaCl2, Ba(HCO3)2, K2SO3, K2S, KCl. Người ta cho từng dung dịch tác dụng với thuốc thử H2SO4 loãng thì có các hiện tượng sau không có hiện tượng gì. tạo kết tủa. tạo khí không màu. tạo khí làm mất màu dung dịch brom. (5) tạo khí, khí tạo kết tủa với dung dịch CuCl2 Hiện tượng xác định Ba(HCO3)2 là A. tạo kết tủa. B. tạo khí không màu. C. tạo khí, tạo kết tủa với dung dịch CuCl2. D. tạo kết tủa và khí không màu. Câu28: Có 5 mẫu kim loại Ba, Mg, Fe, Al, Ag. Chỉ dùng thêm một hoá chất bên ngoài là dd H2SO4 loãng có thể nhận biết được tối đa bao nhiêu kim loại trong các dãy sau? A. Ba, Ag, Fe, Mg. B. Ba, Mg, Fe, Al, Ag. C. Ba, Ag. D. Ba, Ag, Fe. Câu 29:Để nhận biết trong thành phần của khí nitơ có lẫn tạp chất hiđroclorua, ta có thể dẫn khí qua: (1) dd bạc nitrat; (2) dd NaOH; (3) nước cất có vài giọt quỳ tím; (4) nước vôi trong. Phương pháp đúng là: A. chỉ (1). B. (1); (2); (3); (4). C. (1); (3). D. (1), (2), (3). Câu 30: Chỉ có giấy màu ẩm, lửa, và giấy tẩm dd muối X người ta có thể phân biệt 4 lọ chứa khí riêng biệt O2, N2, H2S và Cl2 do có hiện tượng: khí (1) làm tàn lửa cháy bùng lên; khí (2) làm mất màu của giấy; khí (3) làm giấy có tẩm dd muối X hoá đen. Kết luận sai là A. khí (1) là O2; X là muối CuSO4. B. X là muối CuSO4; khí (3) là Cl2. C. khí (1) là O2; khí còn lại là N2. D. X là muối Pb(NO3)2; khí (2) là Cl2. C. ĐÁP ÁN 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 C A A C D D C B C A B A D A A C A B A C 21 22 23 24 25 26 27 28 29 30 C B C A C A B D B C
File đính kèm:
 de_cuong_on_tap_mon_hoa_hoc_lop_12_chuyen_de_phan_biet_mot_s.doc
de_cuong_on_tap_mon_hoa_hoc_lop_12_chuyen_de_phan_biet_mot_s.doc

